Fissaidee 2
1. Dall’atomo di Dalton al modello atomico di Thomson
L’atomo di ThomsonLavoisier e Proust furono tra i primi a scoprire le leggi fondamentali che regolano la formazione dei composti nelle reazioni chimiche.
Per razionalizzare queste leggi l’inglese John Dalton propose la cosiddetta teoria atomica, secondo cui gli atomi sono particelle così piccole da essere invisibili anche al microscopio e ogni elemento chimico è costituito da atomi identici.
È importante sottolineare che in greco il termine atomo significa “indivisibile”, e di conseguenza nella teoria di Dalton gli atomi rappresentano i “mattoni base” di cui è formata la materia.
Tuttavia, alla fine dell’Ottocento i coniugi Pierre e Marie Curie scoprirono la radioattività, cioè quel fenomeno per cui gli atomi di alcuni elementi si trasformano spontaneamente in atomi di elementi più leggeri, emettendo in tale processo delle particelle elettricamente non neutre (particelle alfa o particelle beta).
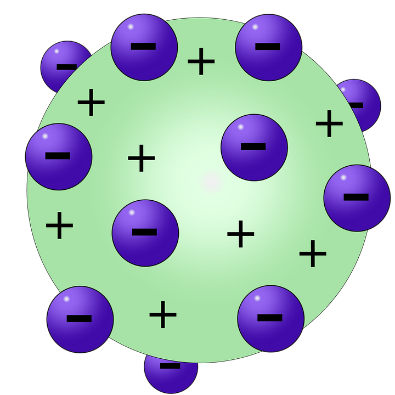
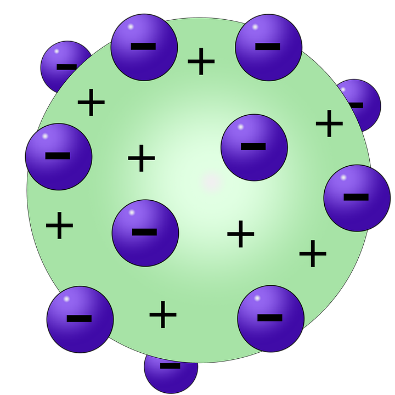
Nello stesso periodo il fisico Joseph John Thomson, durante lo svolgimento di esperimenti con i tubi catodici aveva identificato delle particelle più piccole degli atomi caratterizzate da una carica negativa. A tali particelle è stato dato il nome di elettroni).
Sulla base di tali osservazioni Thomson propose il primo modello dell’atomo caratterizzato da una struttura interna: tale modello, a cui spesso ci si riferisce come modello dell’atomo a “panettone”, prevedeva un atomo composto da una distribuzione di carica positiva diffusa all'interno della quale sono inserite le cariche negative.