Fissaidee 1
| Sito: | Federica Web Learning - LMS |
| Corso: | Scienze chimiche di base |
| Unit: | Fissaidee 1 |
| Stampato da: | Utente ospite |
| Data: | martedì, 26 agosto 2025, 21:26 |
1. La costituzione della materia
La percezione quotidiana porta a condividere l’idea che la materia che ci circonda sia qualcosa di continuo e che si possa suddividere all’infinito, come succede ad esempio al grano o a qualcosa di più duro come un sasso.
Anche se si osserva al microscopio un minuscolo pezzo di un qualsiasi materiale, non si vedono discontinuità evidenti.
D’altra parte, come possiamo classificare gli aeriformi che paiono comportarsi molto diversamente dagli altri stati della materia? Ad esempio, ci possiamo passare in mezzo abbastanza agevolmente. La materia gassosa è quindi discontinua al contrario di quella solida o liquida?
E ancora: come mai i corpi solidi, liquidi e aeriformi manifestano proprietà macroscopiche così diverse?
Per cercare una risposta coerente dobbiamo per prima cosa definire un contesto logico nel quale tutte queste diverse caratteristiche si possano collocare senza contraddizioni.
2. Che cosa è, e perché è utile, un modello
Per dirimere la questione se la materia sia continua o discontinua dobbiamo per prima cosa avanzare un’ipotesi su come la materia sia fatta. Metteremo poi alla prova di esperimenti la nostra ipotesi per verificarne o confutarne la attendibilità.
Nel nostro caso possiamo partire dalla descrizione della materia che fece Democrito. Per Democrito la materia è costituita da particelle semplici che lui denominò atomi (dal greco "indivisibile"). Il sistema proposto dal filosofo greco è il primo esempio di uno strumento che, per la verità solo dopo qualche secolo, verrà con molto profitto usato dagli scienziati: il modello.
Un modello scientifico definisce un quadro concettuale entro il quale è possibile interpretare e rappresentare la realtà, anche quando questa non sia direttamente percepibile con i sensi. Il modello è costituito da assiomi, ossia da definizioni che stabiliamo essere vere e che rappresentano la base per potere interpretare e descrivere i fenomeni osservabili.
Un modello deve non solo consentire di spiegare i fenomeni osservabili, ma anche di predire l’evoluzione di un sistema o l’effetto della variazione di taluni parametri sul fenomeno osservato.
Gli scienziati tengono per buoni questi modelli, ma solo fino a prova contraria! Ossia fino a quando qualche osservazione non porti a contraddire uno o più dei punti del modello.

3. Il modello particellare
Per descrivere, interpretare e, cosa molto importante, rappresentare le proprietà dei corpi faremo uso del modello particellare.
Il modello particellare ipotizza che tutti i corpi materiali siano costituiti di aggregati di particelle intese come entità a sé stanti e separate dalle altre particelle da spazi vuoti più o meno estesi.
Possiamo elencare una serie di assiomi (alcuni di essi già individuati dallo stesso Democrito) ossia di punti che stabiliamo essere veri a priori e che rappresentano la base per potere interpretare e descrivere i fenomeni osservabili.
Possiamo concordare su sette punti che costituiscono il modello particellare per i corpi.
4. I punti del modello particellare /1
Elenchiamo i punti del modello:
- Una particella ha le seguenti caratteristiche: ha dimensione costante è indivisibile, è indeformabile.

- La quantità di materia contenuta in una particella è costante (non cambia).

- Una sostanza è costituita da un solo tipo di particella.
- Un determinato numero di particelle dello stesso tipo equivale sempre alla stessa quantità di sostanza.

- Lo spazio tra una particella e l’altra è vuoto (assenza di materia). Tale spazio ha una estensione variabile a seconda dello stato fisico del corpo.
5. I punti del modello particellare /2
6. Le particelle sono in costante movimento. Esse sono più o meno vincolate le une alle altre e più o meno libere di muoversi a seconda dello stato fisico corpo.
7. Le particelle sono disposte in modo più o meno ordinato e sono più o meno vicine tra loro a seconda dello stato fisico del corpo
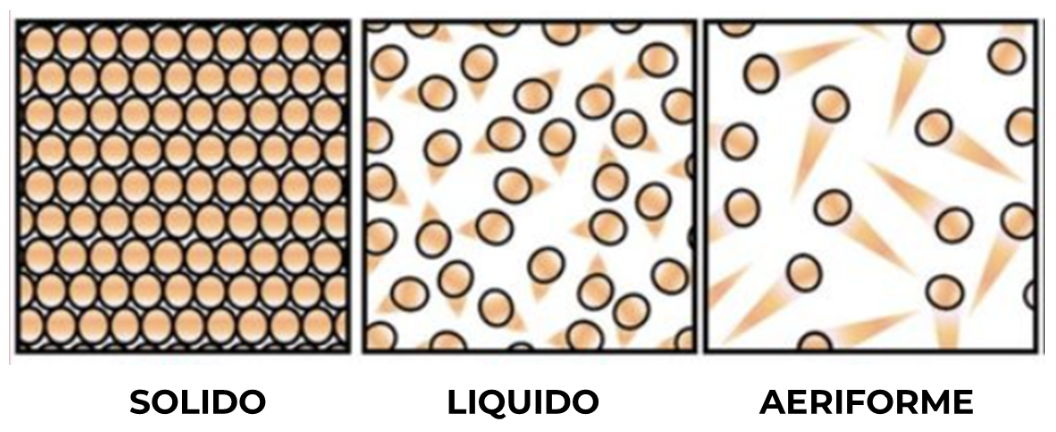
Il modello, per essere utile, dovrà consentirci di distinguere in modo razionale gli stati della materia e di spiegare il passaggio da uno stato all’altro del corpo (trasformazioni di natura fisica) e, in seguito, comprendere le trasformazioni da una sostanza a un'altra (trasformazioni di natura chimica).
I punti dall’1 al 4 del modello consentono di interpretare il comportamento dei corpi sottoposti a sollecitazioni di diversa natura (ad esempio: la compressione, la dilatazione a seguito del riscaldamento, il mescolamento di due corpi, ecc).
I punti successivi, dal 5 al 7, consentono la rappresentazione dei diversi “modi” nei quali il corpo fisico si presenta e consentono di darne una definizione esauriente ed esaustiva.
6. I corpi fisici
Cercheremo ora di comprendere cosa si intende per corpo fisico e come i corpi si possano presentare
È consuetudine suddividere i corpi fisici in tre categorie:
- Corpi solidi, come un lingotto d’oro

- Corpi liquidi, come l’acqua

- Corpi gassosi o aeriformi come il dibromo

A queste tipologie di corpi si possono attribuire proprietà specifiche che ci permettono di identificarli e riconoscerli.
7. I corpi solidi
I Corpi solidi hanno una forma ben definita; occupano uno spazio ben definito; non sono comprimibili.

Ci sono alcuni corpi solidi che, apparentemente, però faticano a stare dentro a queste caratteristiche. Ad esempio, abbiamo corpi granulari: come la sabbia, il sale, la farina; fibrosi, come la lana e spugnosi come la gommapiuma.
Se consideriamo, ad esempio, la sabbia essa non pare avere una forma definita, ad esempio può essere contenuta in una clessidra e attraversare uno stretto passaggio per scorrere nel comparto inferiore. Così il sale fuoriesce attraverso i forellini di una saliera.

Allo stesso tempo una spugna si comprime facilmente, e anche un gomitolo di lana.

Questa osservazione ci porta a riflettere sul fatto che in taluni corpi le proprietà che noi attribuiamo ai solidi siano da rintracciare nelle piccole porzioni che costituiscono questi corpi. Ad esempio, nella sabbia o nel sale sono i singoli granelli che li costituiscono a possedere le proprietà del corpo solido.

8. I corpi liquidi
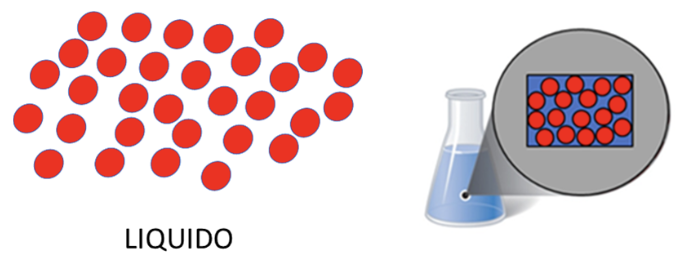
I corpi liquidi si adattano alla forma del recipiente che li contiene, occupano uno spazio ben definito e sono un po’ più comprimibili di quelli solidi, ma comunque sono molto poco comprimibili.
Il liquido più comune è l’acqua che manifesta tutte le proprietà appena richiamate.
Come si può facilmente sperimentare, l’acqua occupa una porzione di spazio ben definito. Ma se il contenitore non c’è, il liquido ne occupa la maggiore estensione disponibile, adattandosi alla superficie da ricoprire.

Ma se consideriamo altri tipi di liquidi possiamo equipararli all’acqua nelle loro proprietà?
Consideriamo per esempio l’olio d’oliva o lo shampoo. Questi due liquidi sono diversi non solo per il colore e le qualità organolettiche (odore e sapore).

Hanno una proprietà importante associata a tutti i corpi liquidi (che si può evidenziare con alcuni semplici esperimenti): la viscosità, proprietà che si evidenzia nella diversa velocità di scorrimento dei liquidi su una superficie.

Alle proprietà dei corpi liquidi aggiungiamo quindi il fatto che possono essere più o meno viscosi. Nella prossima unit parleremo delle caratteristiche dei corpi gassosi.
9. I corpi aeriformi
Vediamo ora quali sono le proprietà specifiche che caratterizzano i corpi aeriformi o gassosi.
Essi non hanno una forma ben definita, non occupano uno spazio ben definito, ma tutto lo spazio a disposizione e sono molto compressibili.
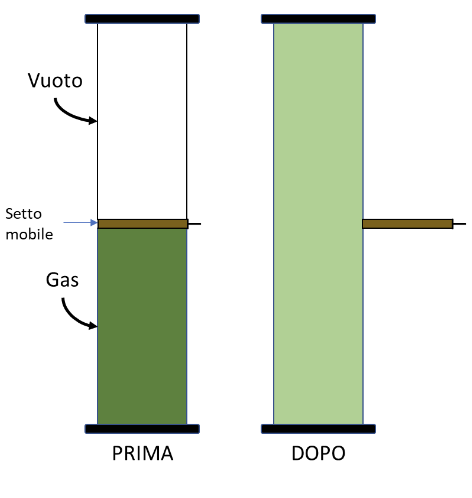
Un corpo gassoso può rapidamente occupare tutto lo spazio disponibile, passando da un contenitore nel quale è presente ad un altro nel quale è fatto il vuoto.
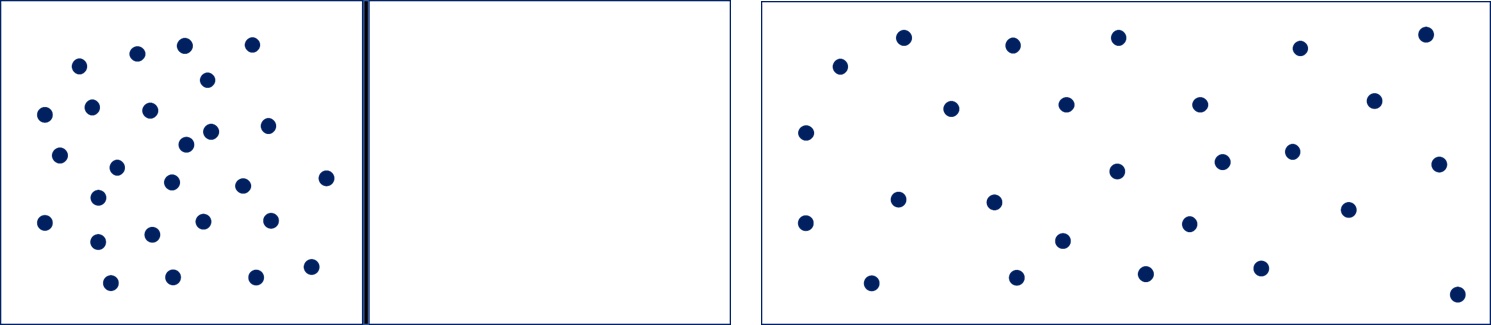
Il fenomeno è evidente se l’esperimento è condotto con un gas colorato. Dopo l’espansione del gas il sistema presenta una colorazione più tenue, indice che le particelle della sostanza si sono distribuite in tutto il volume a disposizione uniforme. La loro quantità è rimasta immutata, ma ora sono distribuite in un volume più grande e di conseguenza anche la colorazione che si osserva è meno intensa.
Abbiamo richiamato in precedenza come sia difficile comprimere solidi e liquidi. Possiamo verificare facilmente la proprietà degli aeriformi di essere facilmente comprimibili, replicando l’esperimento visto in precedenza provando a comprimere l’aria, anziché l’acqua, con una siringa.

L’aria si comprime con sufficiente facilità, anche se più si riduce il volume a disposizione più si avverte una maggiore resistenza. Lasciando il pistone esso torna alla posizione originaria.
La comprimibilità degli aeriformi e il loro non possedere una forma definita si può evidenziare anche con un palloncino non del tutto gonfiato.
10. Il modello particellare all’opera
È giunto il momento di mettere all’opera il nostro modello particellare.
Il primo obiettivo è cercare di rappresentare lo stato fisico di un corpo.
E inizieremo considerando un corpo puro, ossia un materiale costituito da una sola sostanza.
Utilizziamo quindi il punto 3 del nostro modello e rappresentiamo la particella della sostanza con un cerchietto rosso.
Ricordiamoci che stiamo usando un modello, perciò la decisione sulla forma, la dimensione e il colore della particella è del tutto arbitraria: la nostra rappresentazione non è una “fotografia” delle particelle reali, ma solo un modo per potere visualizzare la realtà materiale al livello sub-microscopico e non visibile con i sensi.
![]()
Ora, secondo il punto 1 del modello, tutte le particelle del nostro corpo saranno identiche in forma e dimensione.
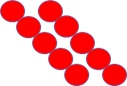
I punti 5, 6, 7 ci aiutano per completare la rappresentazione del corpo nei suoi tre stati.
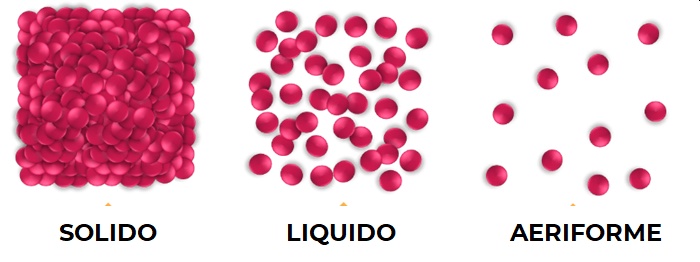
La sostanza allo stato solido presenterà le particelle disposte in maniera ordinata e molto vicine le une rispetto alle altre. Gli spazi vuoti sono molto meno estesi dello spazio occupato dalle particelle. Questa rappresentazione giustifica la “rigidità” di questi corpi dotati di forma e volume definiti.

Lo stato gassoso è rappresentabile con particelle molto distanziate fra loro e disposte in maniera disordinata. Questa rappresentazione giustifica le proprietà specifiche dei corpi gassosi: la comprimibilità e la capacità di occupare tutto lo spazio disponibile. Le particelle dei gas non sono fra loro vincolate e sono libere di muoversi in tutto lo spazio disponibile indipendentemente l’una dalle altre

Lo stato liquido, infine, si troverà in una situazione intermedia. Le particelle non mutano di dimensione, ma sono meno ordinate del solido e meno vincolate del gas. Questo spiega il comportamento dei liquidi (adattabilità alla forma e scarsa compressibilità). Anche la viscosità diversa dei liquidi può essere interpretabile come un diverso grado di vincolo fra le particelle, per esempio, di acqua e di olio.