Fissaidee 2
| Site: | Federica Web Learning - LMS |
| Course: | Biologia di base |
| Unit: | Fissaidee 2 |
| Printed by: | Utente ospite |
| Date: | Tuesday, 26 August 2025, 7:24 PM |
1. Misura del valore energetico di un alimento
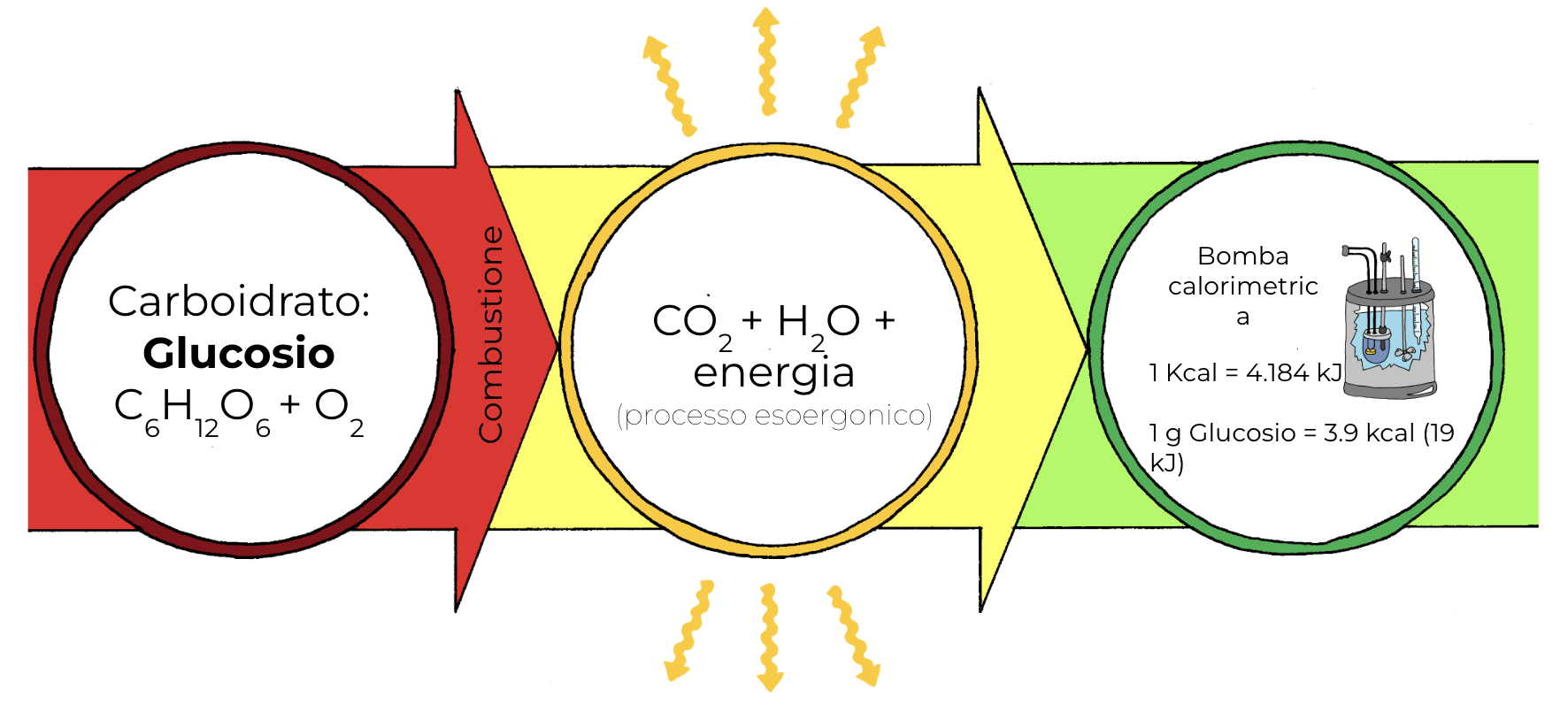
La combustione di una molecola organica come il glucosioUn qualunque alimento è formato da una miscela più o meno complessa di molecole organiche, acqua e sali inorganici. Se sottoposte a combustione, cioè portate ad una temperatura tale da favorire la reazione spontanea con l’ossigeno, le molecole organiche che, come i carboidrati e i lipidi, sono costituite da solo carbonio, idrogeno e ossigeno si trasformeranno interamente in CO2 e H2O. Una volta innescata, la combustione è un processo esoergonico che libera energia sotto forma di calore. Se una quantità nota di un alimento viene portato alla combustione all’interno di un apparato chiamato bomba calorimetrica che misura la quantità di calore rilasciato durante il processo, si ottiene un valore di energia espresso in Kcal o KJ per unità di peso. Una Kcal corrisponde a 4.184 KJ, e la combustione di 1 g di glucosio nella bomba calorimetrica libera 3.9 Kcal, equivalenti a 19 KJ. Il valore medio di 4 Kcal/g è indicativo per l’intera classe dei carboidrati che comprende monosaccaridi come glucosio e fruttosio, disaccaridi come saccarosio e lattosio, e polisaccaridi come l’amido.
2. La respirazione libera energia
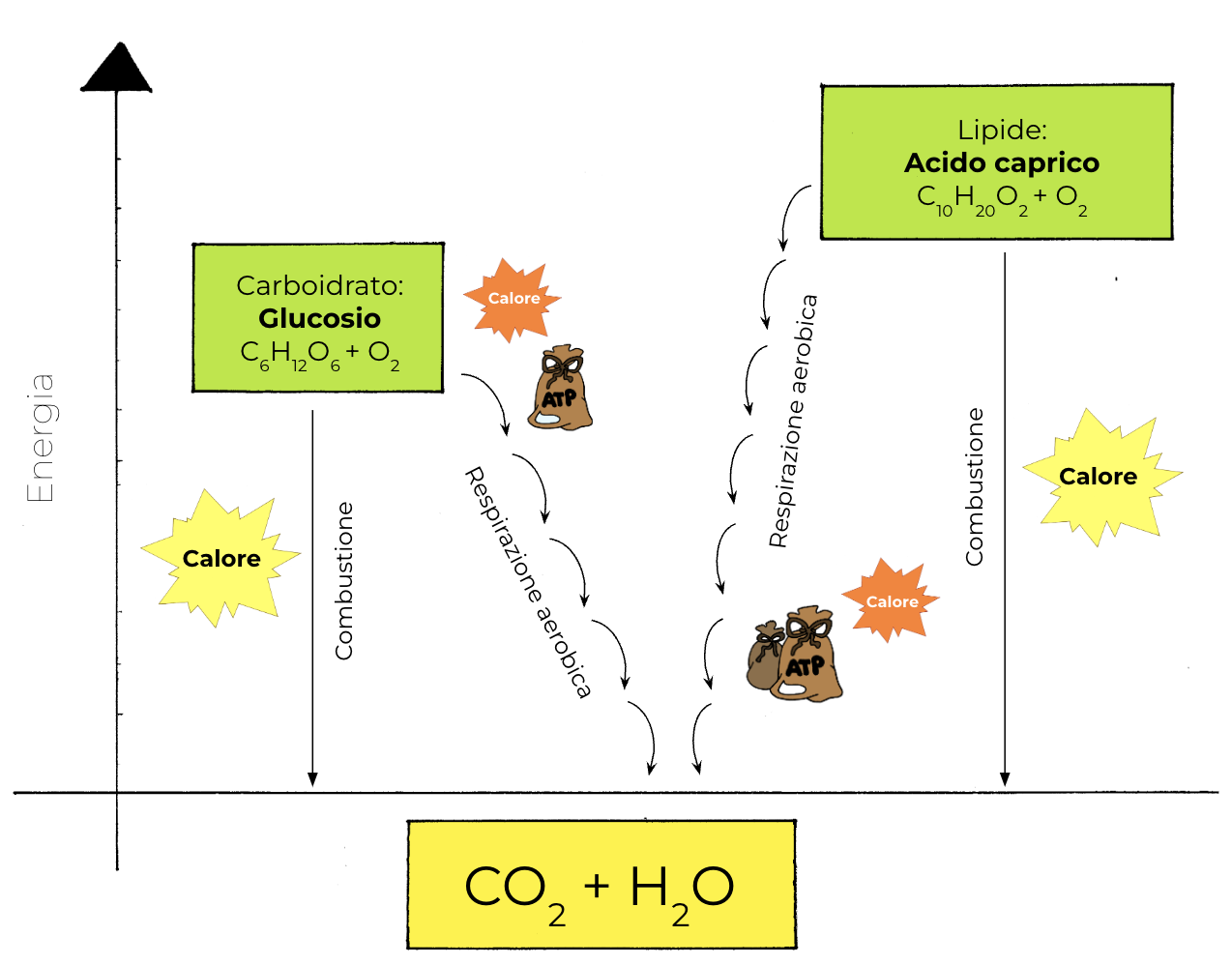
Confronto tra combustione e respirazione aerobica.
Nel confronto tra combustione e respirazione aerobica l’energia liberata è la stessa, ma nella ma nella respirazione aerobica parte di questa energia è conservata come ATP.
Si noti l’asse dell’energia sulla sinistra: in questo tipo di rappresentazione,
le molecole poste più in alto, come l’acido caprico, liberano più energia di
quelle poste più in basso, come il glucosio.
Molecole organiche come per esempio carboidrati o grassi che fanno parte degli alimenti, possono essere metabolizzate all’interno delle cellule attraverso la respirazione aerobica. Ogni reazione metabolica è catalizzata da un enzima diverso che fa sì che la reazione possa avvenire a temperatura ambiente.
Diversamente, la combustione non ha bisogno di enzimi per essere catalizzata, ma richiede alte temperature per essere innescata, dopo di ché procede spontaneamente. Il risultato finale però è lo stesso, e nel caso di molecole come carboidrati e lipidi, i prodotti finali saranno CO2 e H2O. Anche l’energia liberata dalla respirazione sarà la stessa a quella liberata con la combustione, con l’importante differenza che attraverso il metabolismo viene liberata in modo graduale e utilizzata per sintetizzare ATP. Non tutta però, perché almeno la metà andrà inevitabilmente persa sotto forma di calore. Carboidrati e lipidi, nel nostro esempio glucosio e un acido grasso a 10 atomi di carbonio chiamato acido caprico, hanno una diversa composizione in C, H, e O, e per questo liberano diverse quantità di calore durante la combustione. Anche la respirazione aerobica cellulare di glucosio e acido caprico segue vie metaboliche almeno in parte differenti, ed è differente la quantità di ATP che ne deriva.
3. Resa in ATP della respirazione aerobica del glucosio
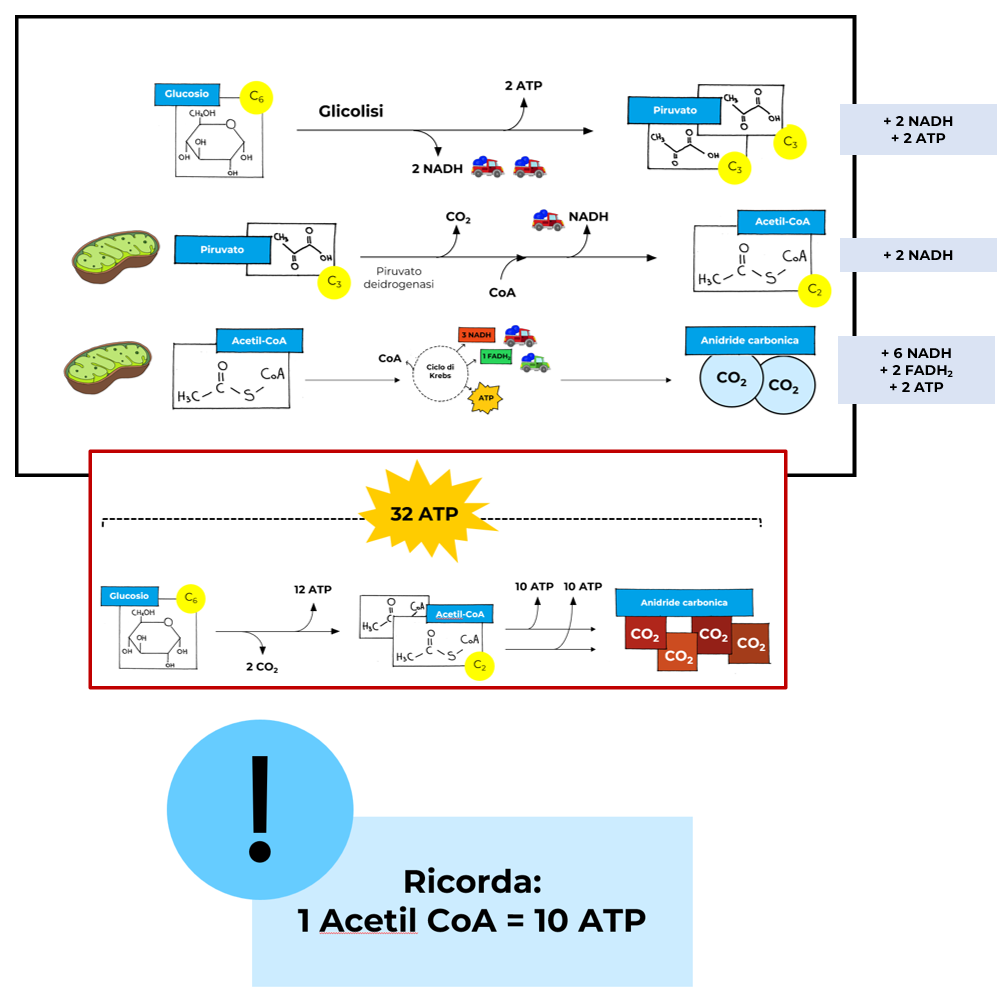
La respirazione aerobica del glucosio
Come si nota in figura, la respirazione aerobica del glucosio può generare 32 molecole di ATP per molecola di glucosio.
Partiamo dai concetti esposti nell’Unità 1 e approfondiamo facendo qualche calcolo:
- Nella glicolisi, il glucosio a 6 atomi di C (C6) viene prima convertito in due molecole di zucchero gliceraldeide-3-fosfato (GAP, C3) con consumo di 2 ATP; successivamente le 2 GAP sono convertite in 2 molecole di piruvato (C3) con produzione di 2 NADH e 4 ATP. Quindi, mediante la glicolisi, da 1 Glucosio (C6) si ottengono 2 Piruvato (C3) + 2 NADH + 2 ATP.
- Nei mitocondri ogni Piruvato (C3) è convertito in acetil-CoA (C2) con liberazione di una CO2 (C1) e produzione di 1 NADH. Per i prossimi calcoli sarà utile ricordare che attraverso i passaggi (1) e (2) da 1 glucosio si ottengono 2 acetil-CoA + 2 CO2 + 4 NADH + 2 ATP.
- Ogni acetil-CoA (C2) viene convertito in 2 CO2 (C1) + 3 NADH + 1 FADH2 + 1 ATP attraverso il ciclo di Krebs.
- Tutto il NADH e il FADH2 prodotto nei tre passaggi precedenti può essere convertito in ATP dall’azione combinata della catena respiratoria, dell’ATP-sintasi e del gradiente protonico che le collega. NADH e FADH2 contribuiscono in modo diverso alla formazione del gradiente protonico, pertanto il fattore di conversione in ATP è diverso: circa 2.5 ATP per il NADH e 1.5 ATP per il FADH2.
- Convertendo tutto il NADH e il FADH2 in ATP, si può calcolare la resa finale:
- da glucosio (C6) a 2 acetil CoA (C2) + 2 CO2 si ottengono 4 NADH e 2 ATP che corrispondono a 4x2.5 + 2 = 12 ATP;
- i 2 acetil-CoA sono convertiti in 4 CO2 (C1) + 6 NADH + 2 FADH2 + 2 ATP, cioè 6x2.5 + 2x1.5 + 2 = 20 ATP (utile tenere a mente che 1 acetil-CoA corrisponde pertanto a 10 ATP).
Globalmente: 32 molecole di ATP per molecola di glucosio respirata.
4. Resa in ATP della respirazione aerobica dell’acido caprico
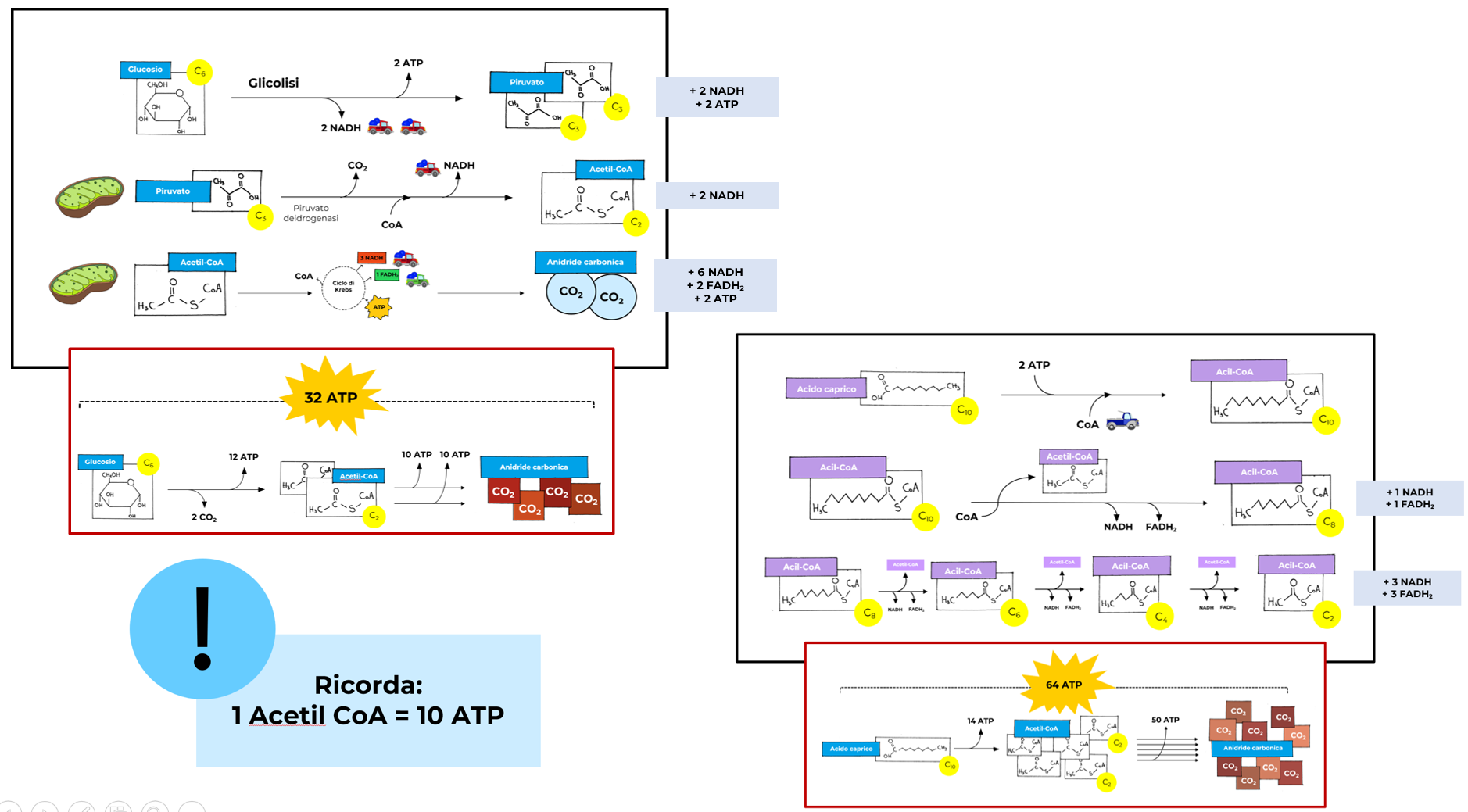
Come in immagine, la respirazione aerobica dell’acido caprico può generare 64 molecole di ATP per molecola di acido grasso.
I grassi della dieta sono in maggior parte costituiti da acidi grassi. L’acido caprico (ACA) è un acido grasso a 10 atomi di carbonio con formula bruta C10H20O2 e peso molecolare simile a quello del glucosio (ACA = 172 Da; GLU = 180 Da). Il metabolismo di un acido grasso inizia con la beta-ossidazione con la quale è interamente convertito in molecole di acetil CoA:
- nella prima reazione della beta ossidazione viene attaccato un Coenzima A (CoA) all’acido grasso consumando due molecole di ATP: ACA + CoA + 2 ATP \( \rightarrow \) ACA-CoA
- in ognuna delle reazioni successive della beta ossidazione, l’acido grasso legato al CoA (acil-CoA, in questo caso ACA-CoA) viene accorciato di due atomi di C che, insieme ad una nuova molecola di Coenzima A, vanno a formare un acetil-CoA (C2-CoA). In ognuna di queste reazioni si produce 1 NADH e 1 FADH2. Dopo 4 reazioni di questo tipo, quel che resta dell’ACA-CoA di partenza sono 5 molecole di acetil-CoA. Quindi, gli acidi grassi possono essere interamente convertiti in acetil-CoA senza perdite di carbonio, a differenza degli zuccheri come il glucosio dove la conversione in acetil-CoA comporta la perdita di 1 CO2 per ogni acetil-CoA prodotto. Globalmente: ACA-CoA + 4 CoA \( \rightarrow \) 5 acetil-CoA + 4x(NADH + FADH2);
Convertendo in ATP e considerando 1 acetil-CoA = 10 ATP (vedi punto precedente), la resa finale della respirazione dell’acido caprico (ACA) diventa:
1 ACA \( \rightarrow \) -2 + 5x10 + 4x4 = 64 ATP.
5. ATP e calorie
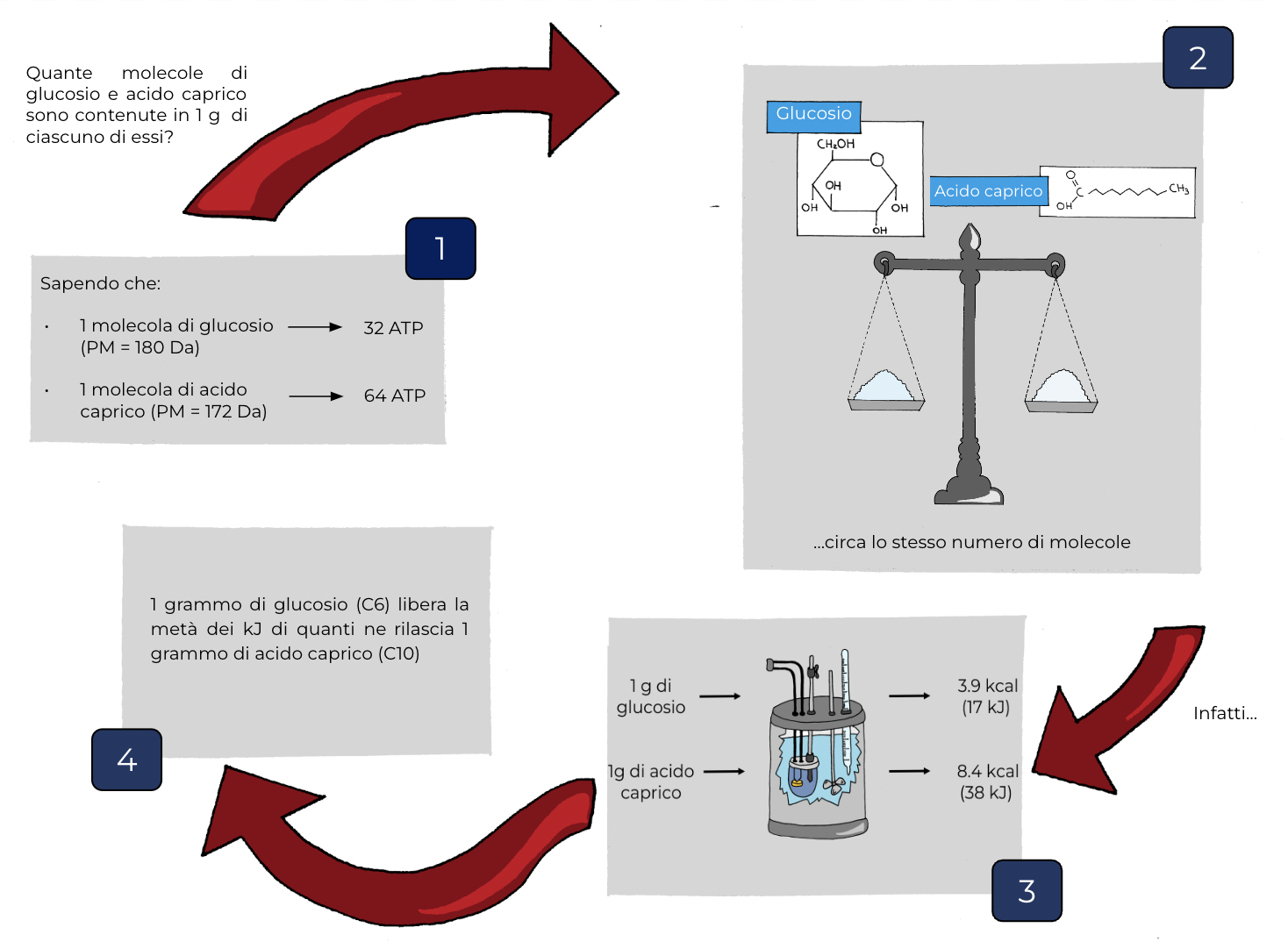
Rapporto tra resa energetica della respirazione aerobica e calore liberato dalla combustione
Siccome il glucosio (GLU) e l’acido caprico (ACA) hanno circa lo stesso peso molecolare, che corrisponde al peso in grammi di una mole (dove 1 mole corrisponde ad un numero fisso di molecole, il numero di Avogadro), allora 1 grammo di ACA conterrà circa lo stesso numero di molecole di 1 grammo di glucosio. Pertanto se 1 molecola di ACA genera il doppio di molecole di ATP (64) rispetto ad una molecola di glucosio (32), anche 1 grammo di ACA dovrebbe liberare circa il doppio di energia rispetto ad 1 grammo di glucosio. In effetti, con la bomba calorimetrica si osserva che 1 g di glucosio libera per combustione 3.9 Kcal (17 kJ) mentre 1 grammo di acido caprico ne libera circa il doppio (8.4 kcal; 38 kJ). Questa misura sperimentale conferma la bontà dei calcoli fatti sulla base della conoscenza del metabolismo.
6. I carboidrati hanno meno calorie dei grassi perché sono più ossidati
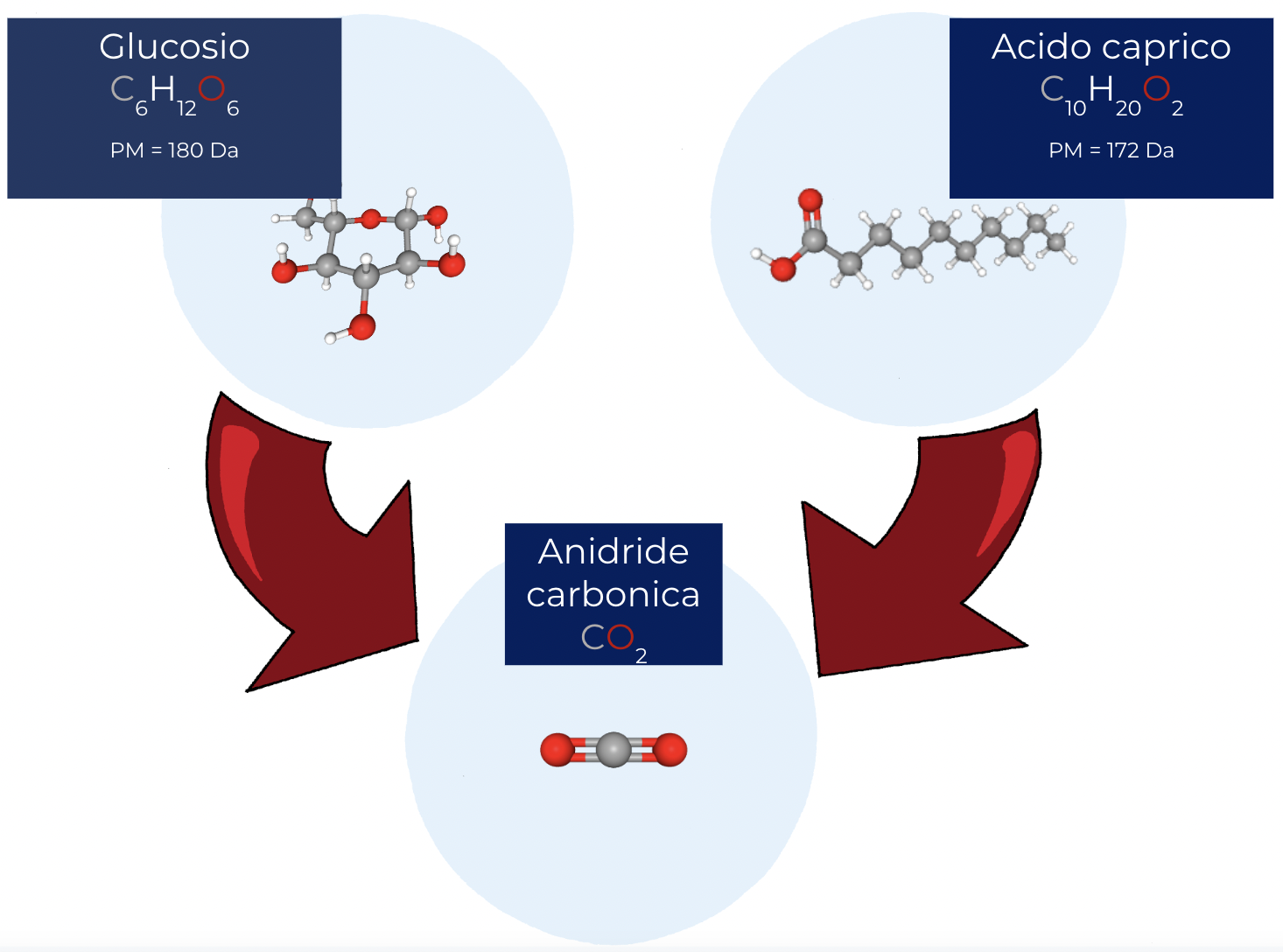
Commentando l'immagine, l’ossigeno (16 Da) pesa molto di più dell’idrogeno (1 Da) e per questo a parità di peso molecolare, lo zucchero, che contiene molto ossigeno (rosso) ha meno atomi, e quindi meno legami, di un acido grasso. Inoltre, molti legami sono già C-O e pertanto non devono essere scissi e riformati per fare la CO2. Ciò riduce a 4 kcal/g la quantità di energia che gli zuccheri possono tipicamente liberare, un po' meno della metà rispetto ai lipidi.
Glucosio e acido caprico hanno simile peso molecolare ma diversa composizione chimica.
Nella molecole rappresentate in figura, le sfere grigie corrispondono ad
atomi di carbonio, le rosse a ossigeno e le bianche a idrogeno.
Le dimensioni delle sfere sono proporzionali al peso molecolare degli atomi che rappresentano: O (16), C (12), H (1).
In un lipide come un acido grasso la maggior parte degli atomi di C sono legati a atomi di H oltre ad essere legati tra loro. In una molecola di acido grasso quindi la maggior parte dei legami è C-C oppure C-H. Per far sì che tutti questi atomi di C vadano a formare la CO2 è necessario che tutti questi legami vengano sostituiti da legami con l’ossigeno (CO2 cioè O=C=O). Come più volte ricordato (vedi Fissaidee dell’Unità 1) questo processo si accompagna al trasferimento di elettroni ad altri atomi di ossigeno (per formare acqua) e genera una certa quantità di energia (9 kcal/g). Negli zuccheri come il glucosio la maggior parte degli atomi di C sono legati ad atomi di H e O oltre che tra di loro (C-H, C-O, C-C).
L’ossigeno pesa molto di più dell’idrogeno e per questo a parità di peso molecolare (come nel caso del confronto tra acido caprico e glucosio), lo zucchero ha meno atomi, e quindi meno legami, di un acido grasso. Inoltre, alcuni legami sono già C-O e pertanto non devono essere rotti e riformati per fare la CO2. Ciò riduce a 4 kCal/g la quantità di energia che gli zuccheri possono tipicamente liberare, un po' meno della metà rispetto ai lipidi.