2. I passaggi di stato e i punti fissi
Le sostanze pure possono essere caratterizzate dai loro punti fissi che corrispondono alla temperatura alla quale la sostanza pura passa da uno stato fisico di aggregazione ad un altro.
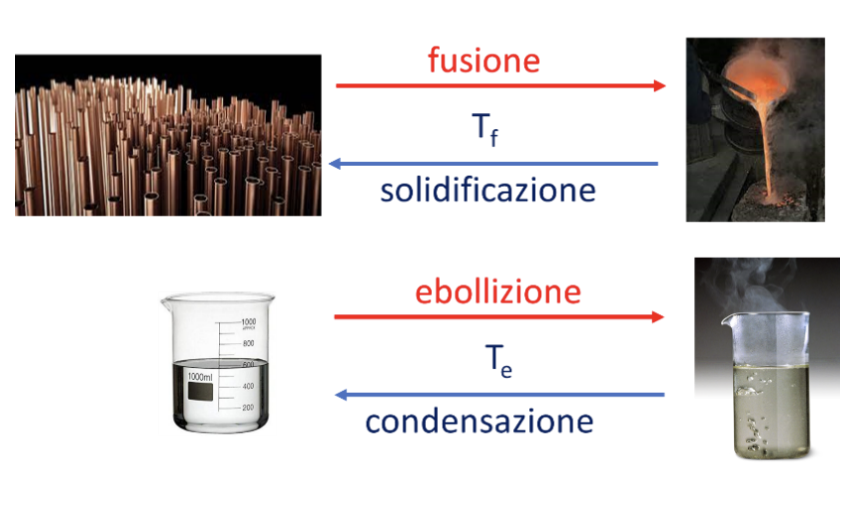
I punti fissi sono la temperatura di fusione (passaggio da solido a liquido) che corrisponde a quella del passaggio opposto: solidificazione e la temperatura di ebollizione (passaggio da liquido a vapore) che corrisponde a quella del passaggio opposto: condensazione).
Le temperature di ebollizione e di fusione rivestono una particolare importanza, perché sono specifiche di ciascuna sostanza e ne permettono un’accurata identificazione.
Il passaggio dallo stato liquido a quello solido è detto solidificazione ed avviene alla stessa temperatura della fusione. Il passaggio dallo stato vapore a quello liquido è detto condensazione ed avviene alla stessa temperatura della ebollizione.
Infine, vi sono altri due passaggi di stato da citare: la sublimazione e il brinamento che indicano, rispettivamente, il passaggio di stato da solido a vapore e il passaggio opposto senza che avvenga il passaggio nello stato liquido intermedio.