Aggregazione dei criteri
Visualizzare
6. Esempio bilanciamento reazioni Red-Ox /3
Step 3. Bilanciare le due semi-reazioni in termini di massa e carica.

Step 4. Bilanciare il numero di elettroni acquistati e ceduti moltiplicando entrambe le semi-reazioni per un numero intero appropriato. Quest’ultimo viene determinato facendo il minimo comune multiplo. Nel caso specifico esso è 10 e quindi la semi-reazione di riduzione va moltiplicata per 2 mentre quella di ossidazione va moltiplicata per 5.
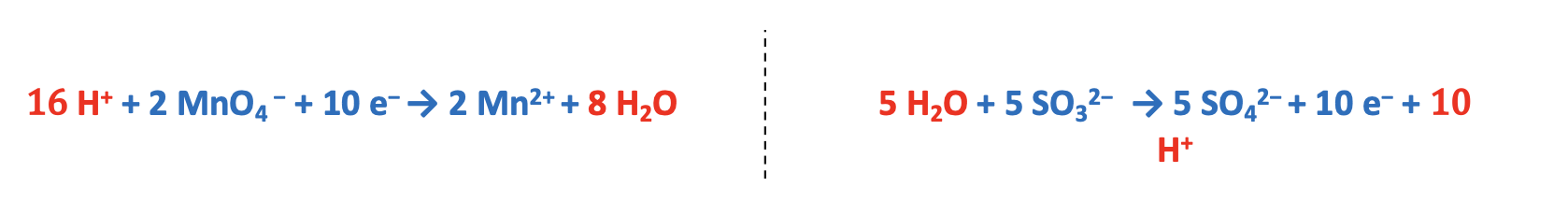
Step 5. Sommare le semi-reazioni e semplificare le specie presenti da entrambi i lati.

