1. Composizione chimica delle proteine
Le proteine sono macromolecole polimeriche formate dalla successione lineare di unità elementari, gli amminoacidi. Gli amminoacidi sono composti del carbonio caratterizzati da un gruppo carbossilico, -COOH, e un gruppo amminico, -NH2, legati ad un atomo di carbonio centrale detto carbonio alfa (a). In tutti gli amminoacidi, al carbonio alfa sono inoltre legati un atomo di idrogeno e una catena laterale, detta gruppo R.
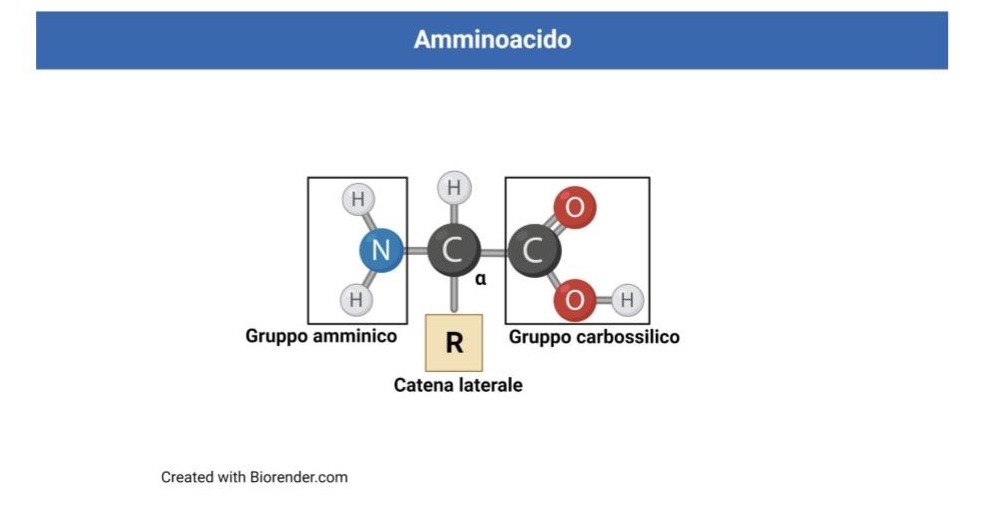
Per la presenza di un gruppo amminico e di un gruppo carbossilico, gli amminoacidi possono comportarsi sia da acidi, sia da basi. Nelle proteine sono presenti 20 tipi di amminoacidi che differiscono per la natura chimica del gruppo R. Nove di questi presentano gruppi R apolari e sono pertanto idrofobici, cioè non formano legami a idrogeno con le molecole di acqua. I restanti 11 amminoacidi presentano gruppi R polari e sono pertanto idrofilici (possono formare legami idrogeno con le molecole dell’acqua).
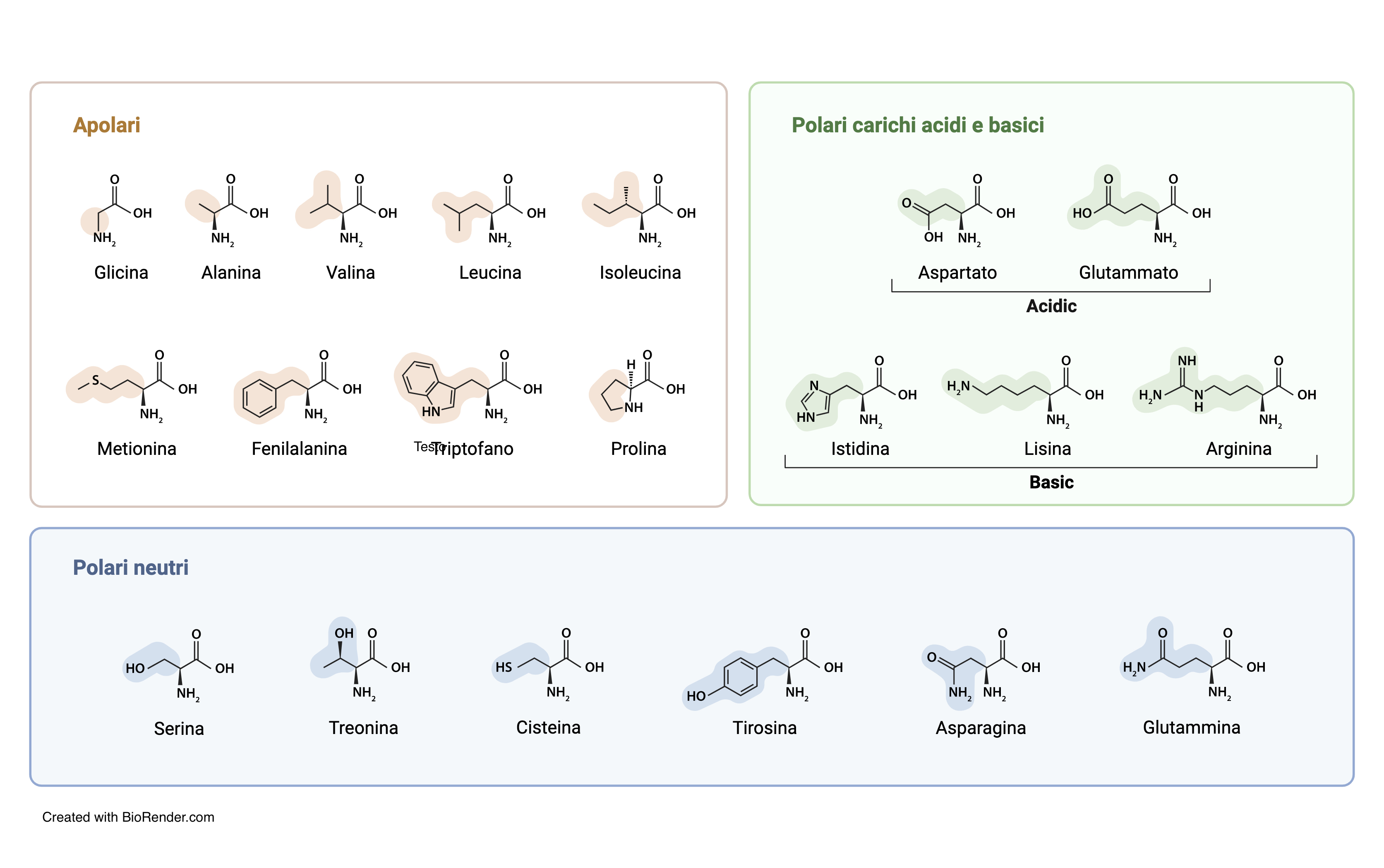
In alcune proteine sono inoltre presenti amminoacidi modificati chimicamente dopo la sintesi della proteina. Nelle proteine, gli amminoacidi sono uniti tra loro da un legame covalente, il legame peptidico, che si forma tra l’atomo di carbonio C del gruppo carbossilico di un amminoacido e l’atomo di azoto N del gruppo amminico dell’amminoacido successivo.
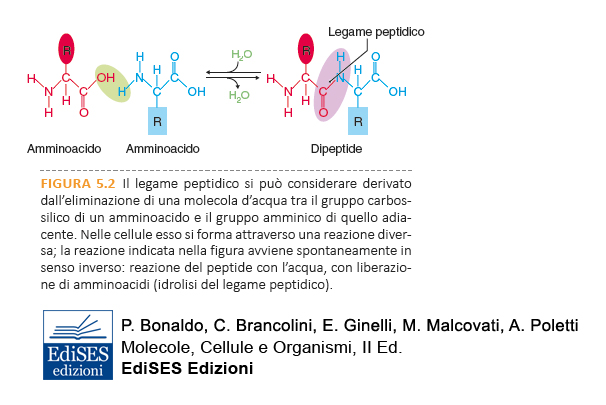
La reazione che porta alla formazione del legame peptidico è una reazione di condensazione, che comporta l’eliminazione di una molecola di acqua. La reazione inversa, di scissione del polimero nelle sue unità elementari, è la reazione di idrolisi che consiste nella rottura del legame covalente tra gli amminoacidi con l’introduzione di una molecola di acqua.
